Durante la reazione PCR, si incontrano spesso alcuni fattori interferenti.
A causa dell'elevatissima sensibilità della PCR, la contaminazione è considerata uno dei fattori più importanti che influenzano i risultati e può produrre risultati falsi positivi.
Altrettanto critiche sono le diverse cause che possono portare a risultati falsi negativi. Se una o più componenti essenziali della miscela di PCR o la reazione di amplificazione stessa vengono inibite o ostacolate, il test diagnostico può risultare compromesso. Ciò può comportare una riduzione dell'efficacia e persino risultati falsi negativi.
Oltre all'inibizione, la perdita di integrità dell'acido nucleico bersaglio può verificarsi a causa delle condizioni di spedizione e/o conservazione precedenti alla preparazione del campione. In particolare, temperature elevate o una conservazione inadeguata possono causare danni alle cellule e agli acidi nucleici. La fissazione di cellule e tessuti e l'inclusione in paraffina sono cause ben note di frammentazione del DNA e rappresentano un problema persistente (vedere Figure 1 e 2). In questi casi, nemmeno un isolamento e una purificazione ottimali risultano efficaci.
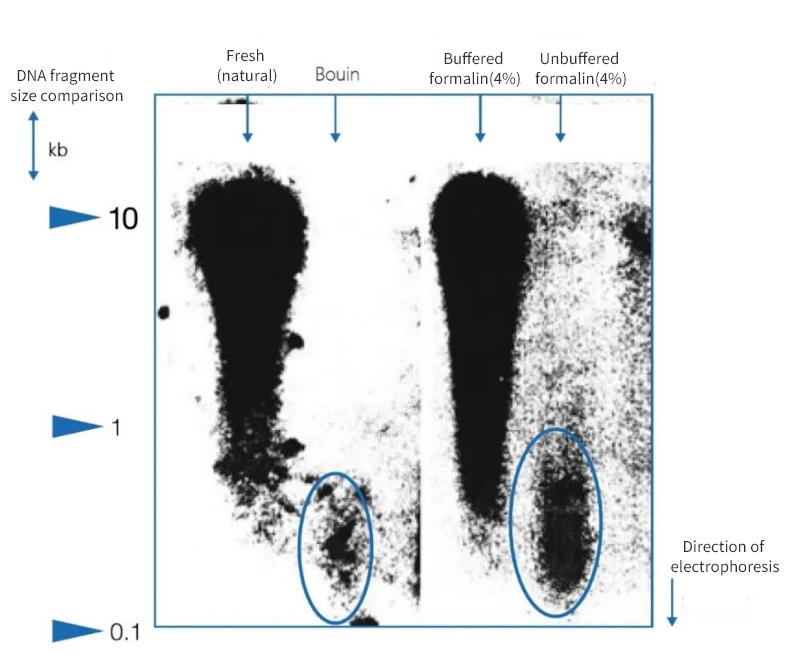
Figura 1 | Effetto dell'immobilizzazione sull'integrità del DNA
L'elettroforesi su gel di agarosio ha dimostrato che la qualità del DNA isolato dalle sezioni di paraffina delle autopsie variava considerevolmente. Negli estratti era presente DNA con diverse lunghezze medie di frammenti, a seconda del metodo di fissazione. Il DNA si è conservato solo se fissato in campioni congelati nativi e in formalina neutra tamponata. L'uso di un fissativo di Bouin fortemente acido o di formalina non tamponata contenente acido formico ha comportato una significativa perdita di DNA. La frazione rimanente risulta altamente frammentata.
A sinistra, la lunghezza dei frammenti è espressa in kilobasi (kbp).
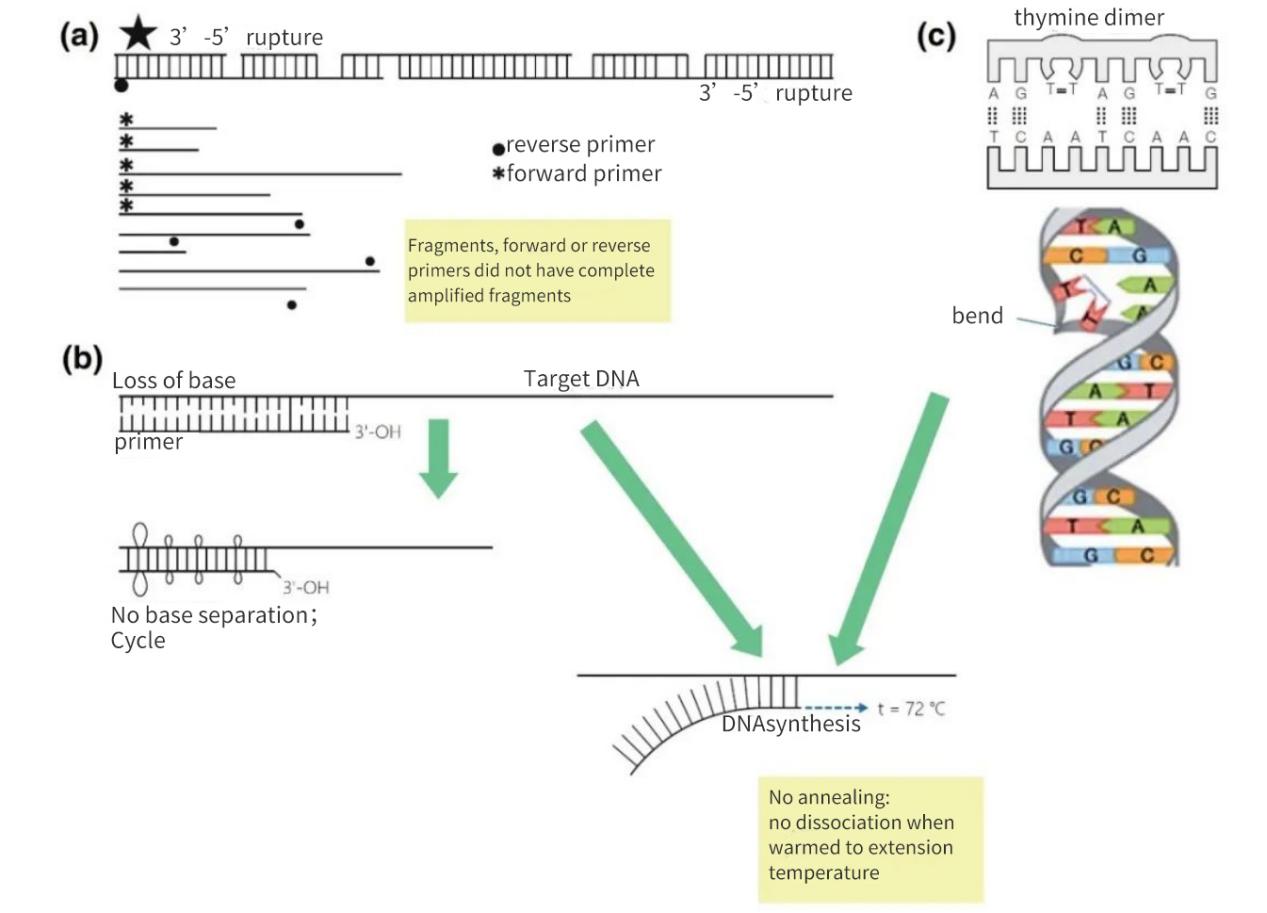
Figura 2 | Perdita di integrità dei bersagli degli acidi nucleici
(a) Un gap 3′-5′ su entrambi i filamenti comporterà una rottura nel DNA bersaglio. La sintesi del DNA avverrà comunque sul piccolo frammento. Tuttavia, se sul frammento di DNA manca un sito di annealing del primer, si verifica solo un'amplificazione lineare. Nel caso più favorevole, i frammenti possono risaturarsi a vicenda, ma le rese saranno basse e al di sotto dei livelli di rilevamento.
(b) La perdita di basi, principalmente dovuta alla depurinazione e alla formazione di dimeri di timidina, porta a una diminuzione del numero di legami H e a una diminuzione della Tm. Durante la fase di riscaldamento prolungata, i primer si denaturano dal DNA della matrice e non si ibridano nemmeno in condizioni meno stringenti.
(c) Le basi di timina adiacenti formano un dimero TT.
Un altro problema comune che si verifica spesso nella diagnostica molecolare è il rilascio non ottimale degli acidi nucleici bersaglio rispetto all'estrazione con fenolo-cloroformio. In casi estremi, ciò può essere associato a falsi negativi. Si può risparmiare molto tempo mediante lisi per ebollizione o digestione enzimatica dei detriti cellulari, ma questo metodo spesso si traduce in una bassa sensibilità della PCR a causa dell'insufficiente rilascio di acidi nucleici.
Inibizione dell'attività della polimerasi durante l'amplificazione
In generale, il termine inibizione viene utilizzato come concetto generale per descrivere tutti i fattori che portano a risultati subottimali nella PCR. In senso strettamente biochimico, l'inibizione si limita all'attività dell'enzima, ovvero riduce o impedisce la conversione substrato-prodotto attraverso l'interazione con il sito attivo della DNA polimerasi o con il suo cofattore (ad esempio, Mg2+ per la Taq DNA polimerasi).
I componenti presenti nel campione o in vari tamponi ed estratti contenenti reagenti possono inibire direttamente l'enzima o intrappolare i suoi cofattori (ad esempio EDTA), inattivando così la polimerasi e portando di conseguenza a risultati PCR ridotti o falsi negativi.
Tuttavia, molte interazioni tra i componenti della reazione e gli acidi nucleici contenenti il target sono anche definite "inibitori della PCR". Una volta che l'integrità della cellula viene compromessa dall'isolamento e l'acido nucleico viene rilasciato, possono verificarsi interazioni tra il campione e la soluzione e la fase solida circostanti. Ad esempio, gli "scavenger" possono legarsi al DNA a singolo o doppio filamento attraverso interazioni non covalenti e interferire con l'isolamento e la purificazione riducendo il numero di target che raggiungono infine il recipiente di reazione della PCR.
In generale, gli inibitori della PCR sono presenti nella maggior parte dei fluidi corporei e dei reagenti utilizzati per i test diagnostici clinici (urea nelle urine, emoglobina ed eparina nel sangue), negli integratori alimentari (componenti organici, glicogeno, grassi, ioni Ca2+) e nei componenti ambientali (fenoli, metalli pesanti).
| Inibitori | Fonte |
| Ioni di calcio | Latte, tessuto osseo |
| Collagene | Tessuto |
| Sali biliari | Feci |
| Emoglobina | Nel sangue |
| Emoglobina | Campioni di sangue |
| Acido umico | Suolo, pianta |
| Sangue | Sangue |
| Lattoferrina | Sangue |
| melanina (europea) | Pelle, capelli |
| Mioglobina | tessuto muscolare |
| Polisaccaridi | Pianta, feci |
| Proteasi | Latte |
| Urea | urina |
| Mucopolisaccaride | Cartilagine, membrane mucose |
| Lignina, cellulosa | Piante |
Gli inibitori della PCR più comuni si trovano nei batteri e nelle cellule eucariotiche, nel DNA non bersaglio, nelle macromolecole che legano il DNA presenti nelle matrici tissutali e nelle apparecchiature di laboratorio come guanti e materiali plastici. La purificazione degli acidi nucleici durante o dopo l'estrazione è il metodo preferito per rimuovere gli inibitori della PCR.
Oggi, diverse apparecchiature di estrazione automatizzate possono sostituire molti protocolli manuali, ma il recupero e/o la purificazione al 100% dei target non è mai stato raggiunto. Potenziali inibitori possono essere ancora presenti negli acidi nucleici purificati o possono aver già avuto effetto. Esistono diverse strategie per ridurre l'impatto degli inibitori. La scelta della polimerasi appropriata può avere un impatto significativo sull'attività degli inibitori. Altri metodi comprovati per ridurre l'inibizione della PCR sono l'aumento della concentrazione della polimerasi o l'aggiunta di additivi come la BSA.
L'inibizione delle reazioni PCR può essere dimostrata mediante l'utilizzo del controllo di qualità interno del processo (IPC).
È necessario prestare attenzione a rimuovere completamente tutti i reagenti e le altre soluzioni presenti nel kit di estrazione, come etanolo, EDTA, CETAB, LiCl, GuSCN, SDS, isopropanolo e fenolo, dall'isolato di acido nucleico mediante un lavaggio accurato. A seconda della loro concentrazione, queste sostanze possono attivare o inibire la PCR.
Data di pubblicazione: 19-05-2023
 中文网站
中文网站