Nat Med | Un approccio multi-omico per mappare il panorama integrato del tumore, del sistema immunitario e del microbioma nel cancro del colon-retto rivela l'interazione del microbioma con il sistema immunitario
Sebbene i biomarcatori per il carcinoma del colon primario siano stati ampiamente studiati negli ultimi anni, le attuali linee guida cliniche si basano unicamente sulla stadiazione TNM (tumore-linfonodi-metastasi) e sull'individuazione di difetti nella riparazione del DNA (MMR) o instabilità dei microsatelliti (MSI) (oltre ai test patologici standard) per determinare le raccomandazioni terapeutiche. I ricercatori hanno notato una mancanza di associazione tra le risposte immunitarie basate sull'espressione genica, i profili microbici e lo stroma tumorale nella coorte di pazienti con carcinoma del colon-retto del Cancer Genome Atlas (TCGA) e la sopravvivenza dei pazienti.
Con il progredire della ricerca, è emerso che le caratteristiche quantitative del carcinoma colorettale primario, tra cui la natura cellulare, immunitaria, stromale o microbica del tumore, sono significativamente correlate agli esiti clinici, ma la comprensione di come le loro interazioni influenzino gli esiti per i pazienti è ancora limitata.
Per analizzare la relazione tra complessità fenotipica ed esito clinico, un team di ricercatori del Sidra Institute of Medical Research in Qatar ha recentemente sviluppato e validato un punteggio integrato (mICRoScore) che identifica un gruppo di pazienti con buone probabilità di sopravvivenza, combinando le caratteristiche del microbioma e le costanti di rigetto immunitario (ICR). Il team ha condotto un'analisi genomica completa di campioni freschi congelati provenienti da 348 pazienti affetti da carcinoma colorettale primario, includendo il sequenziamento dell'RNA dei tumori e del tessuto colorettale sano corrispondente, il sequenziamento dell'intero esoma, il sequenziamento profondo del recettore delle cellule T e del gene 16S rRNA batterico, integrato dal sequenziamento dell'intero genoma tumorale per caratterizzare ulteriormente il microbioma. Lo studio è stato pubblicato su Nature Medicine con il titolo "An integrated tumor, immune and microbiome atlas of colon cancer".

Articolo pubblicato su Nature Medicine
Panoramica di AC-ICAM
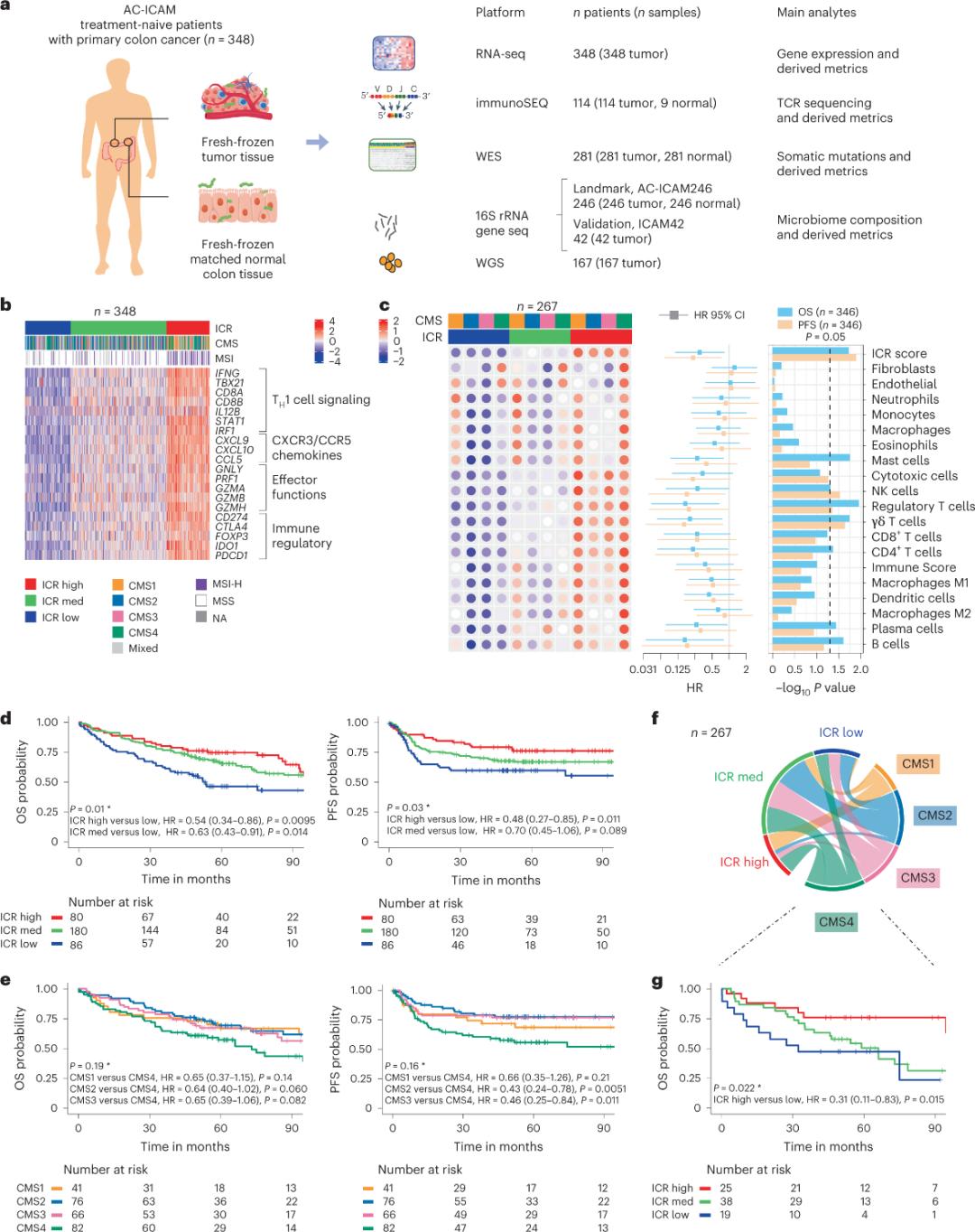
I ricercatori hanno utilizzato una piattaforma genomica ortogonale per analizzare campioni di tumore congelati e il corrispondente tessuto sano del colon adiacente (coppie tumore-normale) provenienti da pazienti con diagnosi istologica di cancro al colon non sottoposti a terapia sistemica. Sulla base del sequenziamento dell'intero esoma (WES), del controllo di qualità dei dati RNA-seq e dello screening dei criteri di inclusione, i dati genomici di 348 pazienti sono stati conservati e utilizzati per analisi successive con un follow-up mediano di 4,6 anni. Il team di ricerca ha denominato questa risorsa Sidra-LUMC AC-ICAM: una mappa e una guida alle interazioni tra sistema immunitario, cancro e microbioma (Figura 1).
Classificazione molecolare mediante ICR
Catturando un insieme modulare di marcatori genetici immunitari per la sorveglianza immunitaria continua del cancro, denominato costante immunitaria di rigetto (ICR), il team di ricerca ha ottimizzato l'ICR condensandolo in un pannello di 20 geni che copre diversi tipi di cancro, tra cui melanoma, cancro alla vescica e cancro al seno. L'ICR è stato anche associato alla risposta all'immunoterapia in una varietà di tipi di cancro, incluso il cancro al seno.
Innanzitutto, i ricercatori hanno convalidato la firma ICR della coorte AC-ICAM, utilizzando un approccio di co-classificazione basato sui geni ICR per classificare la coorte in tre cluster/sottotipi immunitari: ICR alto (tumori caldi), ICR medio e ICR basso (tumori freddi) (Figura 1b). I ricercatori hanno caratterizzato la propensione immunitaria associata ai sottotipi molecolari di consenso (CMS), una classificazione del cancro del colon basata sul trascrittoma. Le categorie CMS includevano CMS1/immunitario, CMS2/canonico, CMS3/metabolico e CMS4/mesenchimale. L'analisi ha mostrato che i punteggi ICR erano correlati negativamente con alcuni percorsi delle cellule tumorali in tutti i sottotipi CMS e correlazioni positive con percorsi immunosoppressivi e correlati allo stroma sono state osservate solo nei tumori CMS4.
In tutti i CMS, l'abbondanza di cellule natural killer (NK) e sottogruppi di cellule T era più elevata nei sottotipi immunitari ICR alti, con maggiore variabilità in altri sottogruppi di leucociti (Figura 1c). I sottotipi immunitari ICR avevano una OS e una PFS diverse, con un aumento progressivo dell'ICR da basso ad alto (Figura 1d), a conferma del ruolo prognostico dell'ICR nel cancro del colon-retto.
Figura 1. Schema dello studio AC-ICAM, firma genica correlata al sistema immunitario, sottotipi immunitari e molecolari e sopravvivenza.
ICR cattura cellule T arricchite nel tumore e amplificate clonalmente
Solo una minoranza di linfociti T che infiltrano il tessuto tumorale risulta essere specifica per gli antigeni tumorali (meno del 10%). Pertanto, la maggior parte dei linfociti T intratumorali viene definita linfociti T "spettatori" (bystander T cells). La correlazione più forte con il numero di linfociti T convenzionali con TCR produttivi è stata osservata nelle sottopopolazioni di cellule stromali e leucociti (rilevate tramite RNA-seq), che possono essere utilizzate per stimare le sottopopolazioni di linfociti T (Figura 2a). Nei cluster ICR (complessivo e classificazione CMS), la clonalità più elevata dei TCR SEQ immunitari è stata osservata nei gruppi ICR-alto e sottotipo CMS1/immune (Figura 2c), con la più alta proporzione di tumori ICR-alto. Utilizzando l'intero trascrittoma (18.270 geni), sei geni ICR (IFNG, STAT1, IRF1, CCL5, GZMA e CXCL10) sono risultati tra i primi dieci geni associati positivamente alla clonalità TCR immuno-SEQ (Figura 2d). La clonalità TCR ImmunoSEQ ha mostrato una correlazione più forte con la maggior parte dei geni ICR rispetto alle correlazioni osservate utilizzando i marcatori CD8+ responsivi al tumore (Figure 2f e 2g). In conclusione, l'analisi di cui sopra suggerisce che la firma ICR cattura la presenza di cellule T arricchite nel tumore e amplificate clonalmente e può spiegarne le implicazioni prognostiche.
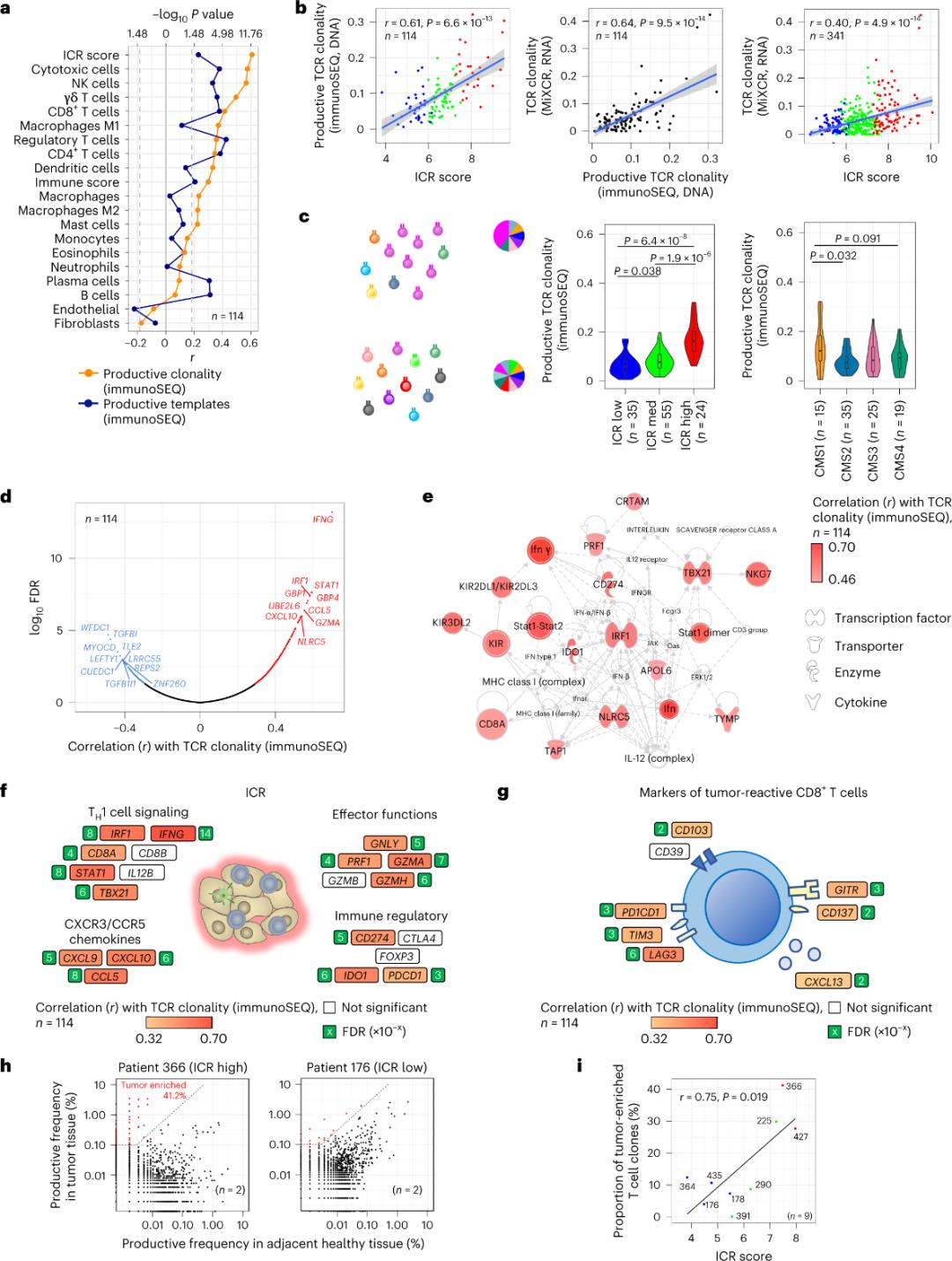
Figura 2. Parametri TCR e correlazione con geni correlati all'immunità, sottotipi immunitari e molecolari.
Composizione del microbioma nei tessuti sani e nei tessuti cancerosi del colon
I ricercatori hanno eseguito il sequenziamento dell'rRNA 16S utilizzando il DNA estratto da tessuto tumorale e tessuto del colon sano corrispondenti, prelevati da 246 pazienti (Figura 3a). Per la convalida, i ricercatori hanno inoltre analizzato i dati di sequenziamento del gene rRNA 16S provenienti da altri 42 campioni tumorali per i quali non era disponibile il DNA normale corrispondente per l'analisi. In primo luogo, i ricercatori hanno confrontato l'abbondanza relativa della flora tra i tumori corrispondenti e il tessuto del colon sano. Il Clostridium perfringens è risultato significativamente aumentato nei tumori rispetto ai campioni sani (Figure 3a-3d). Non è stata riscontrata alcuna differenza significativa nella diversità alfa (diversità e abbondanza di specie in un singolo campione) tra i campioni tumorali e quelli sani, ed è stata osservata una modesta riduzione della diversità microbica nei tumori con ICR-alto rispetto ai tumori con ICR-basso.
Per individuare associazioni clinicamente rilevanti tra profili microbici ed esiti clinici, i ricercatori si sono proposti di utilizzare i dati di sequenziamento del gene 16S rRNA per identificare le caratteristiche del microbioma che predicono la sopravvivenza. Presso l'AC-ICAM246, i ricercatori hanno eseguito un modello di regressione di Cox OS che ha selezionato 41 caratteristiche con coefficienti diversi da zero (associate a un rischio di mortalità differenziale), chiamate classificatori MBR (Figura 3f).
In questa coorte di addestramento (ICAM246), un basso punteggio MBR (MBR<0, basso MBR) è stato associato a un rischio di morte significativamente inferiore (85%). I ricercatori hanno confermato l'associazione tra basso MBR (rischio) e OS prolungato in due coorti validate indipendentemente (ICAM42 e TCGA-COAD). (Figura 3) Lo studio ha mostrato una forte correlazione tra cocchi endogastrici e punteggi MBR, che erano simili nel tessuto tumorale e nel tessuto del colon sano.
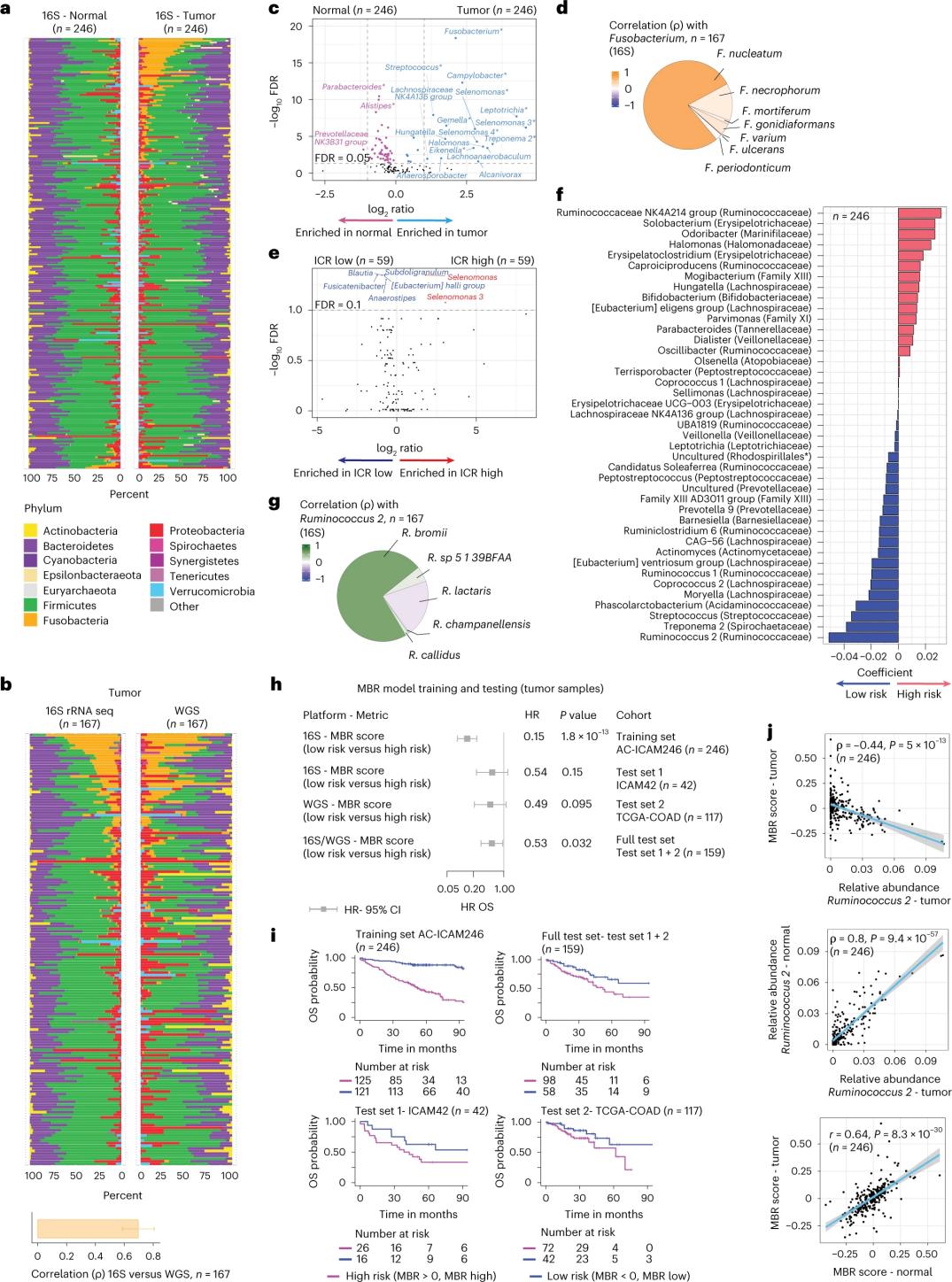
Figura 3. Microbioma nei tessuti tumorali e sani e la relazione con l'ICR e la sopravvivenza del paziente.
Conclusione
L'approccio multi-omico utilizzato in questo studio consente un'individuazione e un'analisi approfondite della firma molecolare della risposta immunitaria nel cancro del colon-retto e rivela l'interazione tra il microbioma e il sistema immunitario. Il sequenziamento profondo del TCR nei tessuti tumorali e sani ha rivelato che l'effetto prognostico dell'ICR potrebbe essere dovuto alla sua capacità di catturare cloni di cellule T arricchiti nel tumore e possibilmente specifici per l'antigene tumorale.
Analizzando la composizione del microbioma tumorale mediante il sequenziamento del gene 16S rRNA in campioni AC-ICAM, il team ha identificato una firma microbica (punteggio di rischio MBR) con un forte valore prognostico. Sebbene questa firma sia stata derivata da campioni tumorali, è stata riscontrata una forte correlazione tra il colon-retto sano e il punteggio di rischio MBR del tumore, suggerendo che questa firma possa riflettere la composizione del microbioma intestinale dei pazienti. Combinando i punteggi ICR e MBR, è stato possibile identificare e validare un biomarcatore multi-omico in grado di predire la sopravvivenza nei pazienti affetti da cancro al colon. Il set di dati multi-omico dello studio fornisce una risorsa per comprendere meglio la biologia del cancro al colon e contribuire alla scoperta di approcci terapeutici personalizzati.
Data di pubblicazione: 15 giugno 2023
 中文网站
中文网站