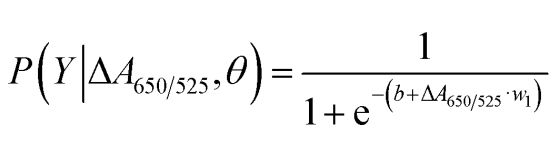La diagnosi precoce del cancro tramite biopsia liquida è una nuova direzione per la rilevazione e la diagnosi del cancro, proposta negli ultimi anni dal National Cancer Institute statunitense, con l'obiettivo di individuare il cancro in fase iniziale o addirittura le lesioni precancerose. È stata ampiamente utilizzata come nuovo biomarcatore per la diagnosi precoce di diverse neoplasie, tra cui il cancro al polmone, i tumori gastrointestinali, i gliomi e i tumori ginecologici.
L'emergere di piattaforme per l'identificazione di biomarcatori del panorama di metilazione (Methylscape) ha il potenziale per migliorare significativamente gli attuali metodi di screening precoce per il cancro, consentendo ai pazienti di accedere alla fase più precoce e trattabile.
Recentemente, i ricercatori hanno sviluppato una piattaforma di rilevamento semplice e diretta per l'individuazione del profilo di metilazione basata su nanoparticelle d'oro decorate con cisteamina (Cyst/AuNPs) combinate con un biosensore basato su smartphone, che consente uno screening precoce rapido di un'ampia gamma di tumori. Lo screening precoce per la leucemia può essere eseguito entro 15 minuti dall'estrazione del DNA da un campione di sangue, con un'accuratezza del 90,0%. Il titolo dell'articolo è "Rilevamento rapido del DNA tumorale nel sangue umano utilizzando AuNPs ricoperte di cisteamina e uno smartphone abilitato all'apprendimento automatico".
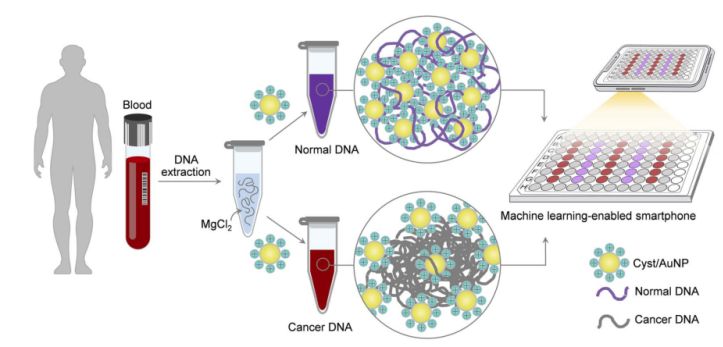
Figura 1. Una piattaforma di rilevamento semplice e veloce per lo screening del cancro tramite componenti Cyst/AuNPs può essere realizzata in due semplici passaggi.
Questo è illustrato nella Figura 1. In primo luogo, è stata utilizzata una soluzione acquosa per sciogliere i frammenti di DNA. Successivamente, sono state aggiunte le Cyst/AuNP alla soluzione risultante. Il DNA normale e quello maligno presentano diverse proprietà di metilazione, che si traducono in frammenti di DNA con differenti modelli di autoassemblaggio. Il DNA normale si aggrega in modo lasco e, infine, aggrega anche le Cyst/AuNP, il che determina lo spostamento verso il rosso delle Cyst/AuNP, in modo che un cambiamento di colore dal rosso al viola sia visibile a occhio nudo. Al contrario, il profilo di metilazione unico del DNA tumorale porta alla produzione di cluster più grandi di frammenti di DNA.
Le immagini delle piastre a 96 pozzetti sono state acquisite utilizzando la fotocamera di uno smartphone. Il DNA tumorale è stato misurato tramite uno smartphone dotato di apprendimento automatico, confrontando i risultati con i metodi basati sulla spettroscopia.
Screening oncologico su campioni di sangue reali
Per ampliare l'utilità della piattaforma di rilevamento, i ricercatori hanno applicato un sensore in grado di distinguere con successo tra DNA normale e canceroso in campioni di sangue reali. I modelli di metilazione nei siti CpG regolano epigeneticamente l'espressione genica. In quasi tutti i tipi di cancro, si è osservata un'alternanza di cambiamenti nella metilazione del DNA e, di conseguenza, nell'espressione dei geni che promuovono la tumorigenesi.
Come modello per altri tumori associati alla metilazione del DNA, i ricercatori hanno utilizzato campioni di sangue di pazienti affetti da leucemia e di soggetti sani per studiare l'efficacia del profilo di metilazione nella differenziazione dei tumori leucemici. Questo biomarcatore basato sul profilo di metilazione non solo supera i metodi di screening rapido per la leucemia attualmente in uso, ma dimostra anche la fattibilità di estendere questo test semplice e diretto alla diagnosi precoce di un'ampia gamma di tumori.
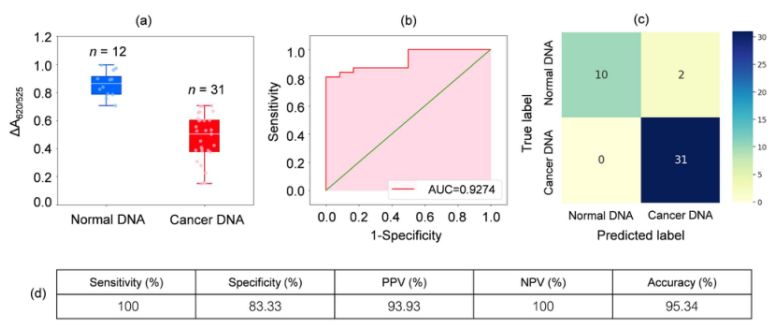
È stato analizzato il DNA di campioni di sangue prelevati da 31 pazienti affetti da leucemia e 12 individui sani. Come mostrato nel box plot in Figura 2a, l'assorbanza relativa dei campioni tumorali (ΔA650/525) era inferiore a quella del DNA dei campioni normali. Ciò era dovuto principalmente all'aumentata idrofobicità che portava a una densa aggregazione del DNA tumorale, la quale impediva l'aggregazione delle Cyst/AuNPs. Di conseguenza, queste nanoparticelle erano completamente disperse negli strati esterni degli aggregati tumorali, il che determinava una diversa dispersione delle Cyst/AuNPs adsorbite sugli aggregati di DNA normali e tumorali. Sono state quindi generate curve ROC variando la soglia da un valore minimo di ΔA650/525 a un valore massimo.
Figura 2.(a) Valori di assorbanza relativi delle soluzioni cisti/AuNPs che mostrano la presenza di DNA normale (blu) e canceroso (rosso) in condizioni ottimizzate
(DA650/525) di box plot; (b) Analisi ROC e valutazione dei test diagnostici. (c) Matrice di confusione per la diagnosi di pazienti normali e affetti da cancro. (d) Sensibilità, specificità, valore predittivo positivo (PPV), valore predittivo negativo (NPV) e accuratezza del metodo sviluppato.
Come mostrato nella Figura 2b, l'area sotto la curva ROC (AUC = 0,9274) ottenuta per il sensore sviluppato ha mostrato elevata sensibilità e specificità. Come si può vedere dal box plot, il punto più basso che rappresenta il gruppo di DNA normale non è ben separato dal punto più alto che rappresenta il gruppo di DNA canceroso; pertanto, è stata utilizzata la regressione logistica per differenziare i gruppi normale e canceroso. Dato un insieme di variabili indipendenti, stima la probabilità che si verifichi un evento, come ad esempio un gruppo canceroso o normale. La variabile dipendente varia tra 0 e 1. Il risultato è quindi una probabilità. Abbiamo determinato la probabilità di identificazione del cancro (P) in base a ΔA650/525 come segue.
dove b=5,3533,w1=-6,965. Per la classificazione del campione, una probabilità inferiore a 0,5 indica un campione normale, mentre una probabilità pari o superiore a 0,5 indica un campione canceroso. La Figura 2c mostra la matrice di confusione generata dalla convalida incrociata leave-it-alone, utilizzata per validare la stabilità del metodo di classificazione. La Figura 2d riassume la valutazione del test diagnostico del metodo, inclusi sensibilità, specificità, valore predittivo positivo (PPV) e valore predittivo negativo (NPV).
Biosensori basati su smartphone
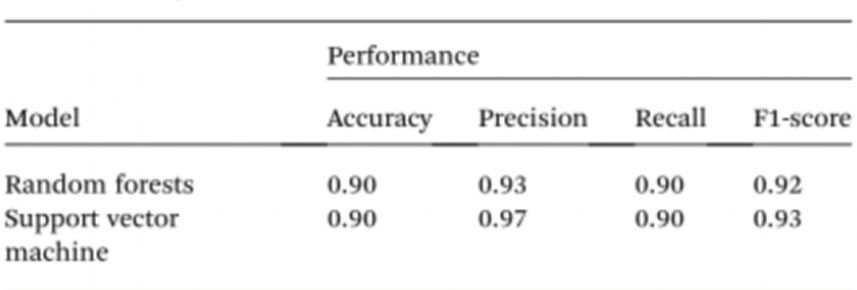
Per semplificare ulteriormente l'analisi dei campioni senza l'utilizzo di spettrofotometri, i ricercatori hanno impiegato l'intelligenza artificiale (IA) per interpretare il colore della soluzione e distinguere tra individui sani e affetti da cancro. A tal fine, la visione artificiale è stata utilizzata per tradurre il colore della soluzione di Cyst/AuNPs in DNA normale (viola) o DNA canceroso (rosso) utilizzando immagini di piastre a 96 pozzetti acquisite con la fotocamera di un telefono cellulare. L'intelligenza artificiale può ridurre i costi e migliorare l'accessibilità nell'interpretazione del colore delle soluzioni di nanoparticelle, senza la necessità di accessori ottici per smartphone. Infine, sono stati addestrati due modelli di apprendimento automatico, Random Forest (RF) e Support Vector Machine (SVM), per la costruzione dei modelli. Entrambi i modelli RF e SVM hanno classificato correttamente i campioni come positivi e negativi con un'accuratezza del 90,0%. Ciò suggerisce che l'utilizzo dell'intelligenza artificiale nel biosensing basato su telefoni cellulari è del tutto fattibile.
Figura 3. (a) Classe target della soluzione registrata durante la preparazione del campione per la fase di acquisizione dell'immagine. (b) Esempio di immagine scattata durante la fase di acquisizione dell'immagine. (c) Intensità del colore della soluzione di cisti/AuNPs in ciascun pozzetto della piastra a 96 pozzetti estratta dall'immagine (b).
Utilizzando Cyst/AuNPs, i ricercatori hanno sviluppato con successo una semplice piattaforma di rilevamento per l'analisi del profilo di metilazione e un sensore in grado di distinguere il DNA normale da quello canceroso utilizzando campioni di sangue reali per lo screening della leucemia. Il sensore sviluppato ha dimostrato che il DNA estratto da campioni di sangue reali è in grado di rilevare rapidamente ed economicamente piccole quantità di DNA canceroso (3 nM) in pazienti affetti da leucemia in 15 minuti, con un'accuratezza del 95,3%. Per semplificare ulteriormente l'analisi dei campioni, eliminando la necessità di uno spettrofotometro, è stato utilizzato l'apprendimento automatico per interpretare il colore della soluzione e distinguere tra individui sani e cancerosi utilizzando una fotografia scattata con un telefono cellulare, raggiungendo un'accuratezza del 90,0%.
Riferimento: DOI: 10.1039/d2ra05725e
Data di pubblicazione: 18 febbraio 2023
 中文网站
中文网站